Содержание
Введение
COVID-19 относится к семейству бета-коронавирусов, которые несут ответственность за возникновение тяжелого острого (SARS HCoV) и ближневосточного (MERS HCoV) респираторных синдромов. До сегодняшнего дня сообщалось о шести различных штаммах коронавируса человека (HCoV) в дополнение к недавно выявленному COVID-19. Штаммы 229E и NL63 HCoV принадлежат к альфа-коронавирусам. Штаммы OC43, HKU1, SARS, MERS и COVID-19 относятся к бета-коронавирусам. SARS и MERS HCoV являются наиболее агрессивными штаммами. По данным ВОЗ, уровень смертности от SARS HCoV составляет 10%, а у MERS HCoV — 36%.
HCoV, как правило, представляют собой одноцепочечные РНК-вирусы с положительной цепью. Очень длинной последовательностью (30000 п.н.) и характеризуются двумя группами белков. Структурные, такие как Spike (S), Nucleocapsid (N) Matrix (M) и Envelope (E). И неструктурные белки, такие как РНК-зависимая РНК-полимераза (RdRp) (nsp12). RdRp является важнейшим ферментом в жизненном цикле РНК содержащих вирусов, включая семейство коронавирусов. Вирус гепатита С (ВГС) и вирус Зика (ZIKV). Активный центр RdRp высококонсервативен и представляет собой два последовательных остатка аспартата, выступающих из структуры бета-витка. Это делает поверхность доступной через нуклеотидный канал (свободные нуклеотиды могут проходить сквозь него).
Врачи отмечают, что применение нуклеотидных ингибиторов в лечении вирусного гепатита С (ВГС) может иметь потенциальные преимущества и в контексте COVID-19. Исследования показывают, что эти препараты способны подавлять репликацию вирусов, что делает их интересными кандидатами для комбинированной терапии. Специалисты подчеркивают, что нуклеотидные ингибиторы могут воздействовать на механизмы, общие для обоих вирусов, что открывает новые горизонты в лечении. Однако врачи также предостерегают о необходимости дальнейших клинических испытаний для оценки безопасности и эффективности таких подходов. Важно учитывать индивидуальные особенности пациентов и возможные взаимодействия с другими лекарственными средствами. Таким образом, мнения врачей подчеркивают необходимость комплексного подхода к лечению, основанного на современных научных данных.

Испытания
В прошлом месяце в Китае начали несколько in vitro и клинических испытаний первого одобренного Национальным управлением по лекарственным средствам Китая (18 февраля 2020 года) лекарственного препарата — Фавилавира. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило различные противовирусные препараты прямого действия против вируса гепатита С (ВГС). Такие как Софосбувир и Рибавирин для применения с целью подавления RdRp. Эти препараты являются производными нуклеотидов, конкурирующих за активный центр RdRp. Полумаксимальная эффективная концентрация (ЕС50) для рибавирина по отношению к COVID-19 составляет 109,5 мкМ. Тогда как его половинная максимальная концентрация ингибирования (IC50) вируса Денге составляет 8 мкМ. Софосбувир демонстрирует 4 мкМ против вируса Зика. Ремдесивир показывает EC90 1,76 мкМ против COVID-19 in vitro.
В настоящем исследовании из-за убедительных доказательств успешного ингибирования RdRp мы сфокусировали свое внимание на доступных в широкой практике нуклеотидных ингибиторах. Гомологическим образом построили модель COVID-19 RdRp после сравнения известных последовательностей с доступными структурами в банке данных протеома. Затем проводили многомерное моделирование молекулярного взаимодействия для оценки некоторых противовирусных препаратов прямого действия (ПППД). Софосбувир, Рибавирин, Ремидисвир, IDX-184 в отношении COVID-19 RdRp. Результаты носят многообещающий характер и предполагают подавление РНК-полимеразы коронавируса доступными в настоящее время терапевтическими средствами.
Результаты и обсуждение
Применение нуклеотидных ингибиторов для лечения вирусного гепатита C (ВГС) в контексте пандемии COVID-19 вызывает активные обсуждения среди специалистов. Многие исследователи отмечают, что эти препараты, изначально разработанные для борьбы с ВГС, могут иметь потенциал в терапии COVID-19 благодаря их способности подавлять репликацию вирусов. Некоторые клинические испытания показывают обнадеживающие результаты, однако мнения разделяются. Некоторые эксперты подчеркивают необходимость дополнительных исследований для оценки эффективности и безопасности таких подходов. В то же время, другие указывают на риск возможных побочных эффектов и взаимодействий с другими лекарственными средствами, используемыми для лечения COVID-19. Таким образом, вопрос о целесообразности применения нуклеотидных ингибиторов остается открытым и требует дальнейшего изучения.

Моделирование RdRp COVID-19
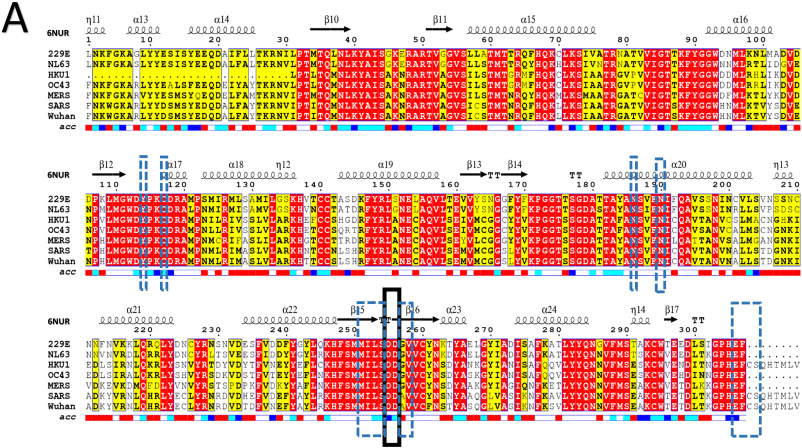
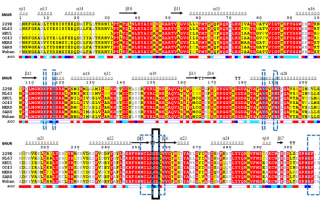
Рисунок 1 А показывает множественное выравнивание последовательностей (MSA) РНК-зависимых РНК-полимераз из различных штаммов HCoV, включая альфа-коронавирусы (229E и NL63) и бета-коронавирусы (OC43, HKU1, SARS, MERS и COVID-19). В верхней части MSA мы показываем вторичную структуру SARS HCoV (PDB ID: 6NUR, цепь A). В нижней части MSA отображаем её доступность. Синими блоками мы выделяем высокодоступные остатки. А белым цветом в нижней части показываем скрытые и недоступные остатки. Прямоугольник с черными штрихами отмечает остатки активных центров (последовательные остатки аспартата D255 и D256).
Активные аспартаты центра выступают из бета-поворота в β15 и β16. Как следует из MSA, активный центр имеет сильный уровень консервативности. Область 5 Å, окружающая D255 и D256, проявляет сильное сродство ко всем HCoV. Это показано синими пунктирными прямоугольниками. Эта область включает в себя Y114, C117, N186, N190, M251, I252, L253, S254, A257, V258, E306, F307, C308 и S309. Остатки активного центра и большая часть окружающей его области 5 Å являются поверхностно доступными. Хотя и могут связываться со свободными нуклеотидами (ATP, GTP, CTP и UTP).
Процентная идентичность
Для COVID-19 RdRp процентная идентичность последовательности по сравнению со штаммами SARS, MERS, OC43, NL63, 229E. И HKU1 HCoV составляет 90.18%, 56.76%, 55.07%, 48.79%, 48.55%, и 48,16% соответственно. Таким образом, SARS HCoV RdRp является наиболее близким штаммом к COVID-19. Полный геном Wuhan SARS-like HCoV имеет идентичность последовательности 89,12%. И 82,34% с изолятом Bat SARS-like coronavirus bat-SL-CoVZC45 и коронавирусом SARS ZS-C соответственно.
Автоматизированное моделирование гомологии построило модель COVID-19 RdRp (801 остаток). Используя SARS HCoV RdRp (PDB ID: 6NUR, цепь A) в качестве гомолога. И модель имеет очень высокую (97,08%) идентичность последовательности, что говорит о её высоком качестве. Карта Рамачандрана показывает 100% остатков в разрешенных регионах, 97,5% — в наиболее благоприятном регионе (рис. 1С). Кроме того, 89,9% остатков имеют средний балл 3D-1D ≤ 0,2 полученный с использованием программного обеспечения Verify 3D. В то время как общий коэффициент качества ERRAT составляет 95,9%.

Взаимодействие ПППД и COVID-19 RdRp
Перед проведением докинг-исследования получают структуры малых молекул, которые должны находиться в оптимизированной трифосфатной форме. Оптимизация выполняется с использованием силового поля MM3. Затем PM6, после чего дальнейшая оптимизация выполняется с помощью теории функционала плотности B3LYP (DFT) основанной на методах расчёта электронной структуры систем квантовой физики и химии. Активный центр аспартата D255 и D256 во время эксперимента стыковки обрабатываются в качестве гибкой структуры.
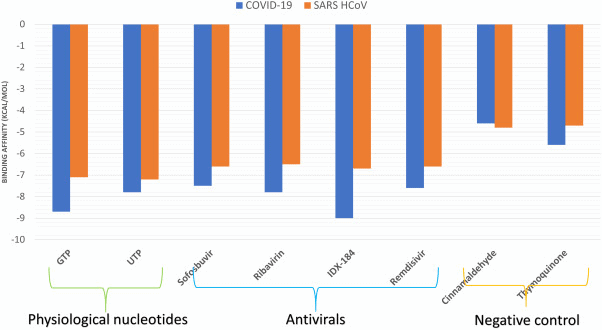
При стыковке с помощью инструментов AutoDock используется сеточный блок размером 30 × 30 × 30 Å с центром в точке (x, y, z) (142.1, 138.7, 150.0) Å. AutoDock Vina использует свою функцию подсчета очков (Vina) для прогнозирования взаимодействия между вышеупомянутыми лигандами и активным центром RdRp. На рис. 2 показаны значения баллов стыковки для COVID-19 (синие столбцы) и SARS HCoVs (оранжевые столбцы). Решенная структура SARS (PDB ID: 6NUR, chain A) используется для стыковки тех же лигандов, чтобы сравнить его энергию связи с энергией связи COVID-19 RdRp. Сеточный блок (30 × 30 × 30 Å) для SARS RdRp центрируется на (141.2, 138.5, 149.4) Å.
Результаты
Как видно из результатов докинга, восемь соединений, включая физиологические GTP и UTP, а также четыре препарата IDX-184, Софосбувир, Рибавирин и Ремидисвир, могут связываться как с COVID-19, так и с SARS HCoV RdRps с хорошей энергией связывания (от -6,5 до -9,0 ккал/моль). Несмотря на то, что SARS HCoV RdRp показывают несколько более высокие энергии связывания по сравнению с COVID-19 RdRp, разница все еще незначительна для Рибавирина, Ремдисивира, Софосбувира и его родительского нуклеотида UTP.
В среднем 0,95 ккал / моль — это разница между энергиями связывания SARS и COVID-19 RdRp для данных соединений. С другой стороны, разница между энергиями связывания COVID-19 и SARS HCoV RdRps с IDX-184 и его родительским нуклеотидом GTP составляет 2,3 и 1,6 ккал/моль соответственно. Кроме того, все испытанные соединения показывают более низкие (лучшие) энергии связывания с COVID-19 RdRp по сравнению с SARS RdRp. Соединения используемые в качестве контроля (циннамальдегид и тимохинон) демонстрируют более низкое связывающее сродство к SARS и COVID-19 RdRp (выше -5,6 ккал/моль).
Исследования комплексов
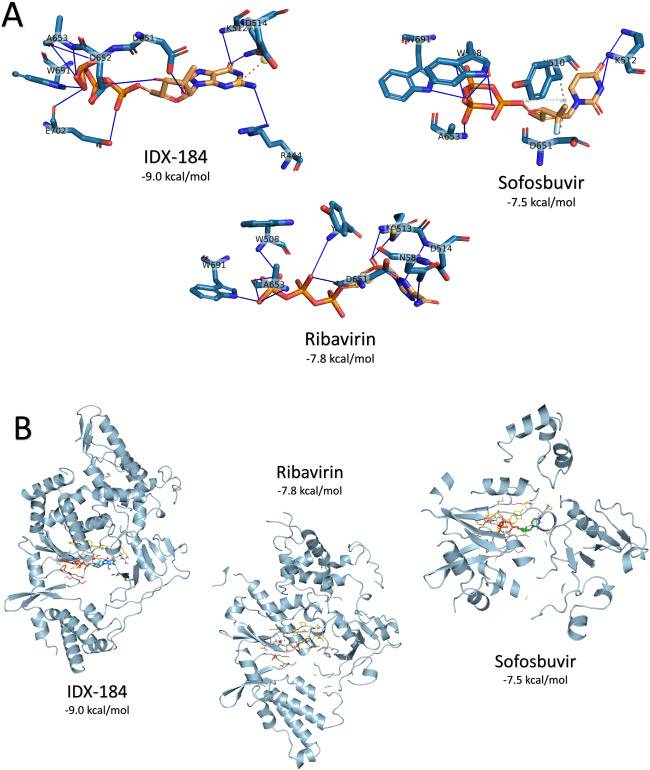
Чтобы проверить возможную причину различий в энергии связей, мы исследовали комплексы взаимодействия, образовавшиеся после стыковки с помощью PLIP. На рис. На рисунке показаны сформированные взаимодействия между препаратами ПППД и RdRp COVID-19 после стыковки. Под каждым комплексом указаны баллы, отражающие силу связывания. Лиганды окрашены в оранжевый цвет, а белковые остатки — в голубой. Водородные связи представляют собой сплошные синие линии, в то время как пунктирные линии представляют гидрофобные взаимодействия. В случае IDX-184 с D514 образуется только один солевой мостик (желтые сферы, соединенные пунктирной линией), который отвечает за повышенную стабилизацию образовавшегося комплекса. Количество водородных связей для IDX-184, софосбувира и рибавирина составляет 11, 7 и 13 соответственно. С другой стороны, IDX-184 и Софосбувир образуют связь между Mg+2 и D652 (два взаимодействия) и E702, соответственно. Это является еще одной причиной стабильности образовавшихся комплексов для IDX-184 и Софосбувира. Кроме того, Софосбувир образовал два гидрофобных взаимодействия с Y510 и D651 RDRP COVID-19.
Подводя итог вышеизложенному, можно сказать, что IDX-184, Софосбувир и Рибавирин могут образовывать плотную связь с RdRp, и, следовательно, нарушать функции важного белка, что приводит к эрадикации вирусной популяции. Кроме того, IDX-184 показывает лучшие результаты в сравнении с Софосбувиром в качестве мощного ингибитора RdRp недавно появившегося штамма COVID-19 HCoV. Дальнейшая изучение взаимодействия вышеупомянутых соединений может привести к получению более мощного препарата, способного остановить вновь возникшее инфекционное заболевание.
Вывод
Возникновение нового штамма коронавируса в городе Ухань вызывает повышенную озабоченность здравоохранения с момента последней вспышки SARS в 2002-2003 году, оставившей более 700 смертей и 8000 случаев заболевания только в Китае. Кроме того, вспышка в ближневосточном регионе, в результате которой погибло более 800 человек и было госпитализировано 2500, имела совершенно иную картину инфицирования (MERS). Настоящее исследование направлено на проверку возможности применения препаратов ПППД, которые широко используют в медицинской практике. Софосбувир, Рибавирин и Ремдисивир показывают многообещающие результаты и могут использоваться против нового штамма COVID-19.
Источники:
- Anti-HCV, nucleotide inhibitors, repurposing against COVID-19
- Life Sciences. Volume 248, 1 May 2020, 117477
Автор: Abdo A. Elfiky. Biophysics Department, Faculty of Sciences, Cairo University, Giza, Egypt. College of Applied Medical Sciences, University of Al-Jouf, Saudi Arabia
Вопрос-ответ
Как нуклеотидные ингибиторы действуют на вирус гепатита С (ВГС)?
Нуклеотидные ингибиторы действуют, блокируя ферменты, необходимые для репликации вируса гепатита С. Они вмешиваются в процесс синтеза вирусной РНК, что приводит к снижению вирусной нагрузки и способствует выздоровлению пациента.
Могут ли нуклеотидные ингибиторы быть эффективны против COVID-19?
Некоторые исследования показывают, что нуклеотидные ингибиторы могут иметь потенциал в борьбе с COVID-19, так как они могут блокировать репликацию вируса. Однако необходимы дополнительные клинические испытания для подтверждения их эффективности и безопасности в лечении COVID-19.
Какие побочные эффекты могут возникнуть при использовании нуклеотидных ингибиторов?
Побочные эффекты могут варьироваться в зависимости от конкретного препарата, но часто наблюдаются такие реакции, как головная боль, тошнота, усталость и изменения в функции печени. Важно, чтобы пациенты находились под наблюдением врача во время лечения.
Советы
СОВЕТ №1
Изучите механизмы действия нуклеотидных ингибиторов, чтобы лучше понять, как они могут воздействовать на вирусы, такие как ВГС и COVID-19. Это поможет вам осознанно подходить к выбору терапии и обсуждать ее с врачом.
СОВЕТ №2
Обсуждайте с вашим лечащим врачом возможные побочные эффекты и взаимодействия нуклеотидных ингибиторов с другими препаратами, которые вы принимаете. Это важно для обеспечения безопасности и эффективности лечения.
СОВЕТ №3
Следите за новыми исследованиями и клиническими испытаниями, связанными с использованием нуклеотидных ингибиторов. Научные данные постоянно обновляются, и новые результаты могут изменить подходы к лечению.
СОВЕТ №4
Не забывайте о важности комплексного подхода к лечению: сочетайте применение нуклеотидных ингибиторов с другими методами профилактики и лечения, такими как вакцинация и соблюдение мер предосторожности, чтобы повысить шансы на успешное выздоровление.